O espectro solar
Introdução
O espectro solar é a distribuição de radiação eletromagnética emitida pelo Sol, abrangendo desde ondas de rádio até raios gama, mas o que mais nos interessa neste momento é a parte visível, que nos permite ver cores vibrantes ao nosso redor.
Nesta aula, exploraremos conceitos essenciais do espectro solar e os espectros de emissão e absorção, as características da luz visível, como acontece a dispersão da luz branca, e como enxergamos as cores dos corpos. Prepare-se para uma jornada educativa que combina ciência e curiosidade!
Espectro Solar
O espectro solar é definido como o conjunto de todas as radiações eletromagnéticas emitidas pelo Sol, que se estende por um amplo intervalo de comprimentos de onda. Ele é geralmente dividido em espectro contínuo, de emissão e de absorção.
Para melhor compreensão, consideremos um exemplo prático: ao passarmos luz solar por um prisma, observamos as diferentes cores que compõem a luz branca, o que ilustra o espectro contínuo. Isso nos ajuda a entender como o Sol emite energia em várias frequências, influenciando fenômenos terrestres como a fotossíntese.

Luz Visível
A luz visível é uma pequena porção do espectro eletromagnético, compreendendo comprimentos de onda entre aproximadamente 400 nanômetros (violeta) e 700 nanômetros (vermelho).
Suas principais características incluem a variação de frequência, que determina as cores que vemos, e a capacidade de ser refratada, refletida e absorvida pelos objetos. Por exemplo, a luz visível é essencial para a visão humana, pois nossos olhos detectam essas ondas e as convertem em impulsos elétricos para o cérebro.
Espectro de Emissão
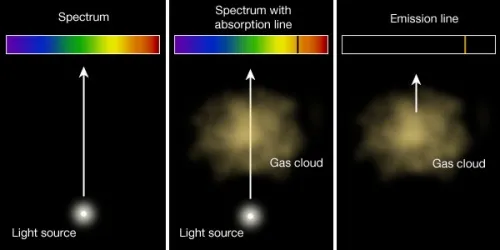
O espectro de emissão ocorre quando átomos ou moléculas em um gás quente e rarefeito são energizados, fazendo com que seus elétrons saltem para níveis de energia mais altos. Ao retornarem aos níveis inferiores, os elétrons liberam energia na forma de fótons com comprimentos de onda específicos, criando linhas brilhantes no espectro. Essas linhas funcionam como assinaturas únicas de cada elemento químico.
As leis de Kirchhoff, formuladas no século XIX, explicam os três tipos fundamentais de espectros: o contínuo (emitido por corpos quentes e opacos), o de emissão (linhas brilhantes de gases quentes e rarefeitos) e o de absorção (linhas escuras sobre um fundo contínuo, produzidas por gases frios à frente de uma fonte quente).

- Cada elemento possui configurações eletrônicas únicas, o que determina os comprimentos de onda exatos emitidos ou absorvidos. Esse processo é governado pelo modelo de Bohr (para átomos simples como o hidrogênio) e, de forma mais completa, pela mecânica quântica, onde a energia dos fótons segue a relação E = hν (ou E = hc/λ), com h sendo a constante de Planck, ν a frequência e λ o comprimento de onda.
Analisando o espectro de emissão de uma estrela, os astrônomos podem identificar elementos ao comparar as linhas observadas com espectros conhecidos de laboratórios terrestres.
Por exemplo, se uma linha específica a 656,3 nm (vermelho) for detectada, sabemos que há hidrogênio presente. Essa técnica é crucial para estrelas distantes, onde amostras físicas são impossíveis de obter.
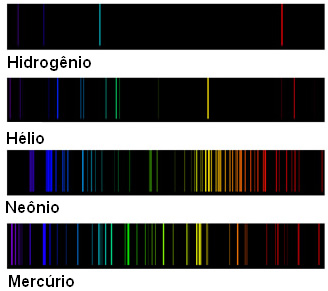
- Exemplos reais: A linha de emissão do hélio (D₃, amarela brilhante) foi descoberta pela primeira vez em 1868 no espectro da cromosfera e protuberâncias solares durante um eclipse, levando à identificação do elemento hélio antes de sua detecção na Terra. Em estrelas massivas, linhas de emissão de elementos pesados como ferro (em estrelas Wolf-Rayet, supernovas ou seus remanescentes) indicam estágios avançados de fusão nuclear, culminando na produção de ferro no núcleo — o ponto final da liberação de energia por fusão.
- Fatores como o efeito Doppler podem deslocar essas linhas, revelando o movimento da estrela. Além disso, a intensidade das linhas indica a abundância de elementos, ajudando a mapear a evolução estelar.
Espectros de Absorção
Os espectros de absorção exibem padrões de linhas escuras no espectro solar, causados pela absorção seletiva de luz em comprimentos de onda específicos por elementos químicos na atmosfera do Sol. Joseph von Fraunhofer, físico e óptico alemão do início do século XIX, foi quem primeiro mapeou sistematicamente essas linhas em 1814, usando um espectrômetro avançado; por isso, elas são conhecidas como linhas de Fraunhofer.
- Essas linhas representam os comprimentos de onda absorvidos por átomos e íons, como o sódio neutro, que cria o famoso dubleto D na região amarela (589 nm).
- Fraunhofer identificou centenas delas — mais de 570 —, rotulando as mais proeminentes com letras; por exemplo, as linhas H e K no violeta (397 nm e ~393 nm), absorvidas pelo cálcio ionizado (Ca II).
- Ao analisar esses espectros, os cientistas determinam a composição química do Sol e de outras estrelas, pois cada elemento apresenta um padrão único de absorção — uma verdadeira impressão digital cósmica.
Dispersão da Luz Branca
A dispersão da luz branca ocorre quando a luz do Sol, que é composta por todas as cores do espectro visível, é separada em suas componentes individuais. Isso acontece devido à variação no índice de refração para diferentes comprimentos de onda, como observado em um prisma de vidro. Um exemplo clássico é o experimento de Isaac Newton, que usou um prisma para decompor a luz branca em um arco-íris (representado na Imagem 1).
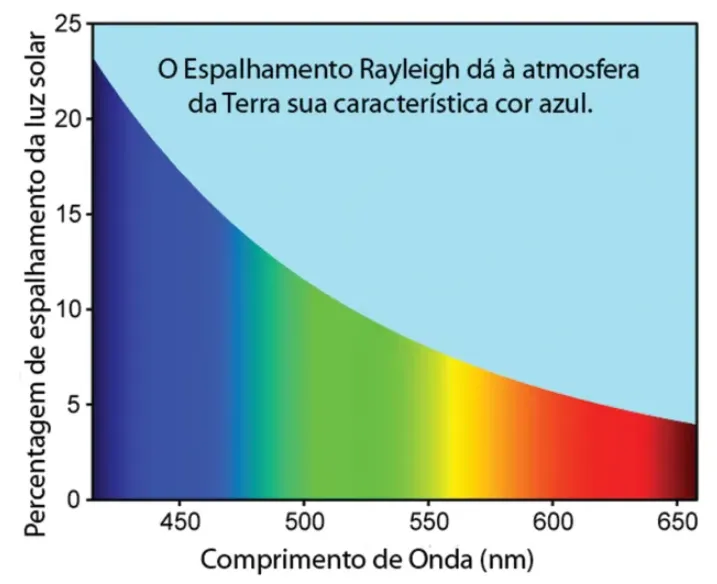
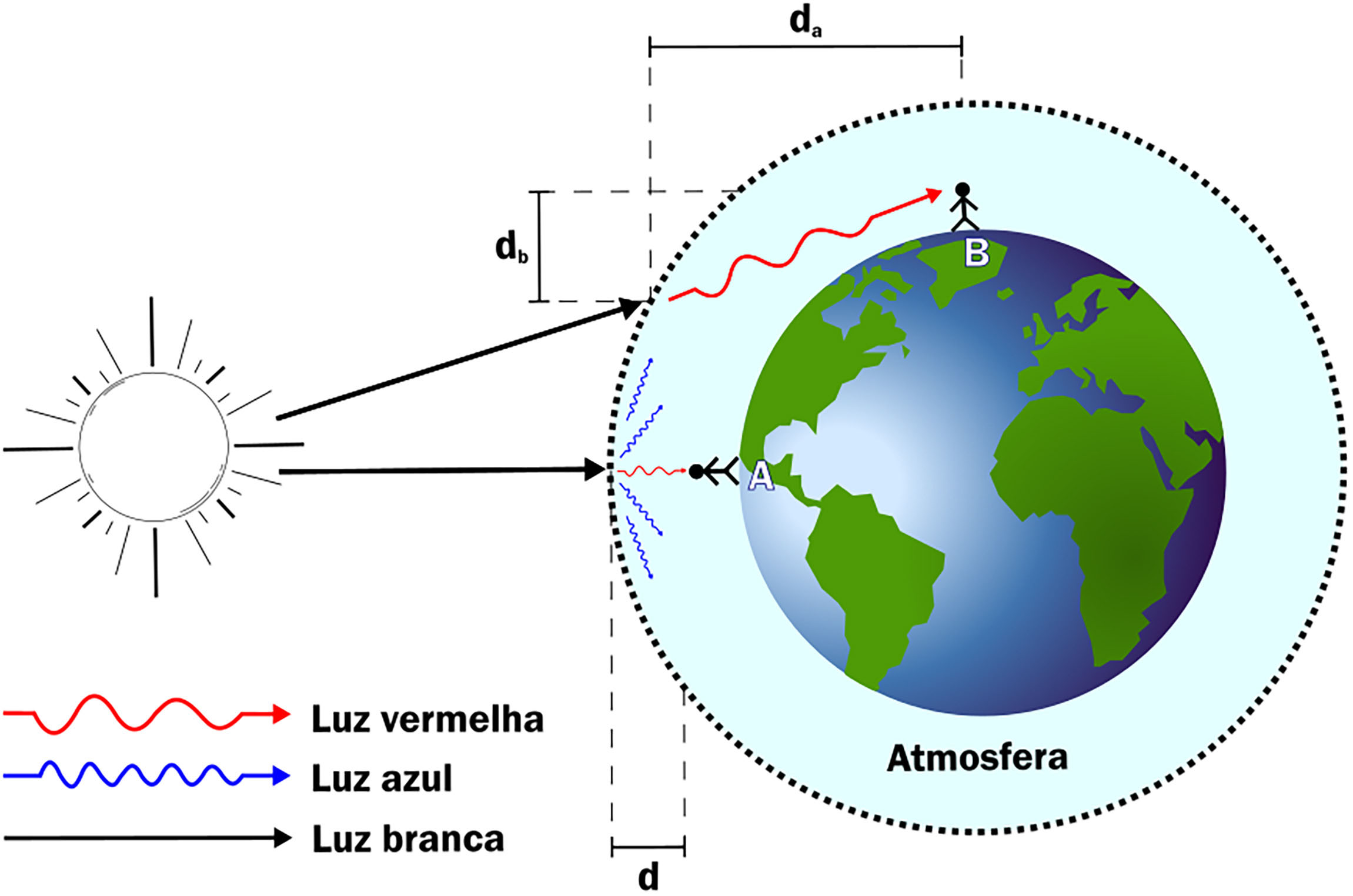
Quando a luz branca incide em um meio como a água ou o vidro, as ondas de menor comprimento (violeta) são refratadas mais que as de maior comprimento (vermelho), resultando na separação das cores. Isso também explica o céu azul durante o dia, devido à dispersão de Rayleigh, onde a atmosfera dispersa mais a luz azul que as outras cores.

Como Enxergamos as Cores dos Corpos
Enxergamos as cores dos corpos devido à interação da luz visível com a superfície dos objetos. Quando a luz incide sobre um objeto, parte é absorvida e parte é refletida. Nossos olhos, equipados com cones sensíveis a diferentes comprimentos de onda, interpretam a luz refletida como cor.
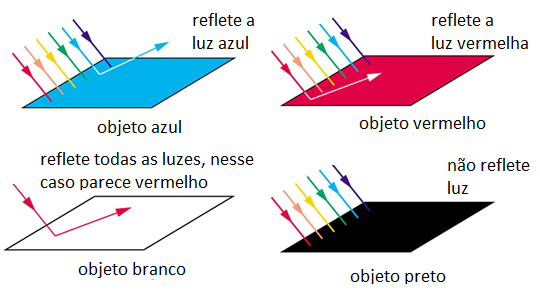
Por exemplo, uma maçã parece vermelha porque absorve a maior parte da luz visível, exceto a vermelha, que é refletida para nossos olhos.
Conclusão
O espectro solar nos revela a beleza e a complexidade da luz. Compreendemos agora as características da luz visível, o fenômeno da dispersão e como enxergamos cores nos objetos cotidianos. Essa aula destaca a importância de estudar o espectro solar para avanços em ciências como a astronomia e a ótica.
[2] Sala de Demonstrações de Física. Disponível em: https://demonstracoes.fisica.ufmg.br/artigos/ver/107/18.-Espalhamento-da-luz
[3] Penn State Astronomy & Astrophysics. Disponível em: https://courses.ems.psu.edu/astro801/content/l3_p6.html
[4] Khan Academy. Disponível em: https://pt.khanacademy.org/science/9-ano/materia-e-energia-as-ondas/as-cores/a/cor-luz-e-cor-pigmento
[5] Getty Images. Disponível em: https://www.livescience.com/physics-mathematics/refraction-is-then-all-there-is-to-it-how-isaac-newtons-experiments-revealed-the-mystery-of-light
[6] Por Alchemist-hp www.pse-mendelejew.de - Obra do próprio, CC BY-SA 2.0 de, https://commons.wikimedia.org/w/index.php?curid=7601144
[7] FOGAÇA, Jennifer Rocha Vargas. "Espectros de Emissão e de Absorção e Leis de Kirchhoff"; Brasil Escola. Disponível em: https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm.
[8] Rev. Bras. Ensino Fís. 48. 2026. Por que o céu é azul? Um experimento sobre espalhamento Rayleigh. Disponível em: https://doi.org/10.1590/1806-9126-RBEF-2025-0171